::: ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยา :::

|
|
............................................................................................................................................. ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยา
.
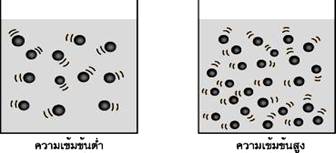
1.ความเข้มข้นของสารตั้งต้น กรณีที่สารตั้งต้นเป็นสารละลาย ถ้าสารตั้งต้นมีความเข้มข้นมากจะเกิดเร็ว
เนื่องจากตัวถูกละลายมีโอกาสชนกันมากขึ้นบ่อยขึ้นในทางตรงกันข้าม ถ้าเราเพิ่มปริมาตรของสารละลายโดยความเข้มข้นเท่าเดิม อัตราการเกิดปฏิกิริยาจะเท่าเดิม
.
.
.
.
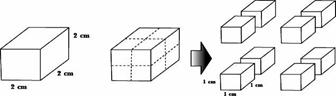
2.พื้นที่ผิวสัมผัส กรณีที่สารตั้งต้นมีสถานะเป็นของแข็ง สารที่มีพื้นที่ผิวสัมผัสมากจะทำปฏิกิริยาได้เร็วขึ้น
เนื่องจากสัมผัสกันมากขึ้นใช้พิจารณากรณีที่สารตั้งต้นมีสถานะของแข็ง ดังภาพ
.
.
.
.
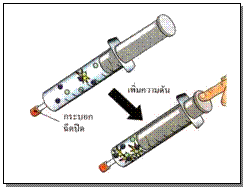
3.ความดัน กรณีที่สารตั้งต้นมีสถานะเป็นก๊าซ ถ้าความดันมากปริมาตรก็ลดลง และปฏิกิริยาก็จะเกิดได้เร็ว
เนื่องจากอนุภาคของสารมีโอกาสชนกันมากขึ้นบ่อยขึ้นในพื้นที่ที่จำกัดนั่นเอง ดังภาพ
.
.
.
.
4.อุณหภูมิ การที่อุณหภูมิของสารตั้งต้นเพิ่มขึ้นอัตราการเกิดปฏิกิริยาจะเพิ่มขึ้น
เนื่องจากเมื่ออุณหภูมิสูงขึ้นโมเลกุลของสารในระบบจะมีพลังงานจลน์สูงขึ้นและมีการชนกันของโมเลกุลมากขึ้น
.
.
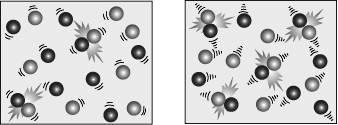
ปฏิกิริยาที่อุณหภูมิต่ำ.......................ปฏิกิริยาที่อุณหภูมิสูง
.
.
5.ตัวเร่งปฏิกิริยา (Catalyst)หมายถึงสารเคมีที่ช่วยทำให้อัตราการเกิดปฏิกิริยาเร็วขึ้น
เนื่องจากตัวเร่ง จะช่วยในการลดพลังงานกระตุ้นโดยช่วยปรับกลไกในการเกิดปฏิกิริยาให้เหมาะสมกว่าเดิม
โดยจะเข้าไปช่วยตั้งแต่เริ่มปฏิกิริยาแต่เมื่อสิ้นสุดปฏิกิริยาจะ กลับมาเป็นสารเดิม
.
.
6.ธรรมชาติของสาร เนื่องจากสารมีแรงยึดเหนี่ยวซึ่งแตกต่างกัน
โดยปกติสารประกอบไอออนิกจะเคลื่อนที่ได้เร็วกว่าสารประกอบโควาเลนต์
ดังนั้นสารประกอบไอออนิกจะเกิดปฏิกิริยาเร็วกว่าสารประกอบโควาเลนต์
.
.
.
.
แหล่งอ้างอิง
|














