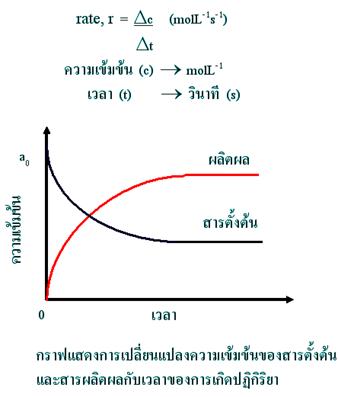
::: อัตราการเกิดปฏิกิริยาเคมี :::

|
|
................................................................................................................................ อัตราการเกิดปฏิกิริยาเคมี .
. (ที่มารูป ::: http://www.tps.ac.th/~narin/basicchem/index_files/image101.jpg )
อัตราการเกิดปฏิกิริยาเคมี
หมายถึง ปริมาณสารตั้งต้นที่หายไปต่อหนึ่งหน่วยเวลาหรือปริมาณผลิตภัณฑ์ที่เกิดขึ้นต่อหนึ่งหน่วยเวลา
.
ในขณะที่ปฏิกิริยาดำเนินไป สาร A และสาร B เป็นสารตั้งต้นถูกใช้ไปดังนั้นความเข้มข้นของสาร A และ B จะลดลง
.ดังนั้นเมื่อเขียนความสัมพันธ์ระหว่างอัตราการเกิดปฏิกิริยาในรูปของสารต่างๆ
อัตราการเกิดปฏิกิริยาเคมี = ปริมาณของสารตั้งต้นที่ลดลง/ เวลา
ประเภทของอัตราการเกิดปฏิกิริยา
*อัตราเร็วเฉลี่ย หมายถึง
อัตราเร็วโดยเฉลี่ย ตั้งแต่เริ่มต้น จนปฏิกิริยาเกิดขึ้นในช่วงเวลาหนึ่ง ( หาได้จากการทดลอง) อัตราเร็วของปฏิกิริยาที่ตำแหน่งใดตำแหน่งหนึ่ง ( หาจากค่าความชันของกราฟระหว่างปริมาณสารกับเวลา)
วิธีการวัดอัตราการเกิดปฏิกิริยา
การวัดอัตราการเกิดปฏิกิริยาจะพิจารณาจากการวัดปริมาณของสารตั้งต้นหรือสารผลิตภัณฑ์ได้
1.ถ้าในปฏิกิริยาเกี่ยวข้องเป็นแก๊ส อาจจะวัดอัตราการเกิดปฏิกิริยาจากปริมาณของแก๊สที่เกิดขึ้น
2.ถ้าในปฏิกิริยาเกี่ยวข้องกับสารที่มีสี อาจจะวัดอัตราการเกิดปฏิกิริยาจากความเข้มข้นของสีที่ลดลงของ 3.ถ้าในปฏิกิริยาเกี่ยวข้องกับสารละลาย จะวัดอัตราการเกิดปฏิกิริยาจากความเข้มข้นของสารละลายที่เปลี่ยนไป . .
แหล่งอ้างอิง
http://www.electron.rmutphysics.com/science-news/index.php?option=com_co... http://sites.google.com/site/suwitklong/rate . .
|