::: ทฤษฎีที่ใช้อธิบายปฏิกิริยาเคมี :::

.
.

.
.
.
.
ทฤษฎีที่ใช้อธิบายปฏิกิริยาเคมี
.
การเกิดปฏิกิริยาเคมี เป็นการเปลี่ยนแปลงของสารที่ได้ผลิตภัณฑ์ของสารที่แตกต่างจากสารเดิมโดยอาจ สังเกตจากการเปลี่ยนสีของสาร การเกิดตะกอน หรือการเกิดกลิ่นใหม่ ทฤษฎีที่ใช้อธิบายปฏิกิริยาเคมี มีอยู่ 2 ทฤษฎี คือ
.
.
1. ทฤษฎีการชน (The Collision Theory) ปฏิกิริยาเคมีจะเกิดขึ้นได้ ก็ต่อเมื่ออนุภาคของสารตั้งต้นต้องมาปะทะกันหรือมาชนกัน และการชนกันนั้นมีทั้งการชนที่ประสบผลสำเร็จ ดังภาพ
.
.
.

แบบจำลองการเกิดปฏิกิริยาเคมีตาม ทฤษฎีการ
.
.
จากทฤษฎีการชนจะสังเกตได้ว่า การชนที่ประสบผลสำเร็จหรือการชนที่ทำให้เกิดสารผลิตภัณฑ์จะต้องประกอบด้วยองค์ประกอบที่สำคัญสองอย่าง คือ
1. ทิศทางของการชน (orientation of collision)
2. พลังงานของการชน (energy of collision)
.
.
1.ทิศทางของการชน
.............สารตั้งต้นเป็นแก๊สหรือของเหลวคงเกิดปฏิกิริยาได้ง่าย เพราะอนุภาคที่เป็นแก๊สหรือของเหลวเคลื่อนที่ได้ง่าย โดยเฉพาะแก๊ส ถ้าเราใช้ความดันช่วยบีบให้อนุภาคเข้ามาชิดกันมากขึ้น ปฏิกิริยาก็จะยิ่งเกิดได้ง่ายมากขึ้น
.............สารตั้งต้นเป็นแก๊สหรือของเหลวคงเกิดปฏิกิริยาได้ง่าย เพราะอนุภาคที่เป็นแก๊สหรือของเหลวเคลื่อนที่ได้ง่าย โดยเฉพาะแก๊ส ถ้าเราใช้ความดันช่วยบีบให้อนุภาคเข้ามาชิดกันมากขึ้น ปฏิกิริยาก็จะยิ่งเกิดได้ง่ายมากขึ้น
.

.
.
.
.
2. พลังงานของการชน
อนุภาคชนกันในทิศทางที่เหมาะสมแล้วก็ยังไม่เพียงพอ สิ่งที่สำคัญมากกว่านั้นก็คือ พลังงาน เพราะถึงแม้ว่าอนุภาคจะชนกันในทิศทางที่ถูกต้องแต่พลังงานของอนุภาคมีไม่มากเพียงพอ ก็ไม่อาจที่จะเกิดปฏิกิริยาได้
.
.
.
.
.
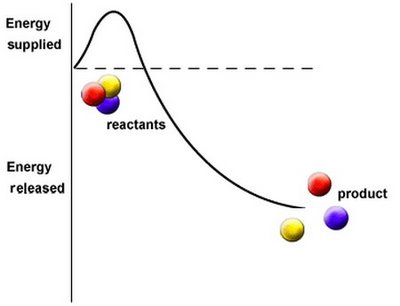
การเกิดปฏิกิริยาเคมีย่อมเกี่ยวข้องกับการสลายพันธะเดิมและสร้างพันธะใหม่ ซึ่งการสลายพันธะเดิมต้องใช้พลังงานอย่างแน่นอน พลังงานในที่นี้ก็คือพลังงานที่เราเรียกว่า พลังงานก่อกัมมันต์ (activation energy)
.
.
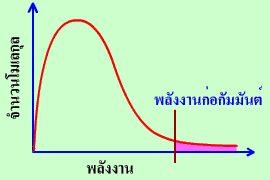
พลังงานก่อกัมมันต์ (activation energy)
.
พลังงานกระตุ้น = Activation energy) ย่อว่า Ea คือ พลังงานจำนวนน้อยที่สุดที่เกิดจากการชนของอนุภาคของสารตั้งต้นแล้วทำให้เกิดปฏิกิริยาเคมี ใช้หน่วยเป็น kJ/mol หรือ kcal/mol
.
.
.
.
.
.
ลักษณะสำคัญของพลังงานก่อกัมมันต์
.
1. ปฏิกิริยาเคมีที่ต่างชนิดกัน พลังงานก่อกัมมันต์ต่างกัน
2. ปฏิกิริยาที่มีพลังงานก่อกัมมันต์ต่ำ ปฏิกิริยาจะเกิดง่ายหรือเร็วกว่าปฏิกิริยาที่มีพลังงานก่อกัมมันต์สูง
3. พลังงานก่อกัมมันต์ไม่เกี่ยวข้องกับอัตราการเกิดปฏิกิริยา คือ ปฏิกิริยาที่มีพลังงานก่อกัมมันต์ต่ำ ปฏิกิริยานั้นอาจจะมีอัตราการเกิดปฏิกิริยา ...............เร็วหรือสูงก็ได้
4. พลังงานก่อกัมมันต์ไม่เกี่ยวข้องกับพลังงานของปฏิกิริยา
1. ปฏิกิริยาเคมีที่ต่างชนิดกัน พลังงานก่อกัมมันต์ต่างกัน
2. ปฏิกิริยาที่มีพลังงานก่อกัมมันต์ต่ำ ปฏิกิริยาจะเกิดง่ายหรือเร็วกว่าปฏิกิริยาที่มีพลังงานก่อกัมมันต์สูง
3. พลังงานก่อกัมมันต์ไม่เกี่ยวข้องกับอัตราการเกิดปฏิกิริยา คือ ปฏิกิริยาที่มีพลังงานก่อกัมมันต์ต่ำ ปฏิกิริยานั้นอาจจะมีอัตราการเกิดปฏิกิริยา ...............เร็วหรือสูงก็ได้
4. พลังงานก่อกัมมันต์ไม่เกี่ยวข้องกับพลังงานของปฏิกิริยา
.
.
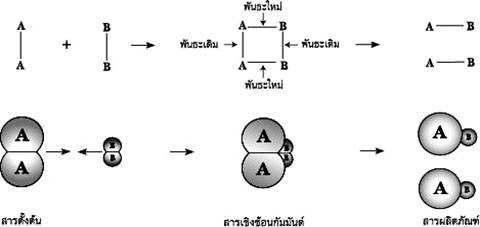
2. ทฤษฎีแอกติเวเตดคอมเพลกซ์หรือทฤษฎีสภาวะทรานซิชัน (The Activated Complex Theory or The Transition State Theory) เป็น ทฤษฎีที่ดัดแปลงมาจากทฤษฎีการชน โดยทฤษฎีนี้จะกล่าวถึงการชนอย่างมีประสิทธิภาพของสารตั้งต้นในลักษณะที่ เหมาะสม โดยจะเกิดเป็นสารประกอบใหม่ชั่วคราว ที่เรียกว่า สารเชิงซ้อนกัมมันต์ (Activated Complex) ซึ่งในระหว่างการเกิดสารชนิดนี้พันธะเคมีของสารตั้งต้นจะอ่อนลง และเริ่มมีการสร้างพันธะใหม่ระหว่างคู่อะตอมที่เหมาะสม จนในที่สุดพันธะเก่าจะถูกทำลายลงอย่างสิ้นเชิง และจะมีพันธะใหม่ถูกสร้างขึ้นมาแทนที่ ดัง แบบจำลองการเกิดปฏิกิริยาเคมีต่อไปนี้
.
.
.
.
แบบจำลองการเกิดปฏิกิริยาเคมีตาม ทฤษฎีแอกติเวเตดคอมเพลกซ์
.
.
.
.
.
แหล่งอ้างอิง
.
.
.
.
.
.
.
.
.










