::: ปฏิกิริยาในแบตเตอรี่ :::

.
.

.
.
ปฏิกิริยาในแบตเตอรี่
.
( ปฏิกิริยาในเซลล์ประเภททุติยภูมิ )
.
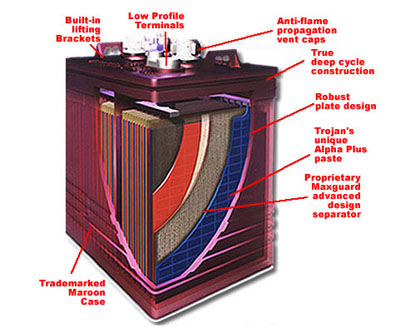
.
( ที่มารูป ::: http://www.4weupload.com/images/712010InsideTrojanBattery.jpg )
.
.
เซลล์ทุติยภูมิ (Secondary Battery)
.
หรือโดยทั่วไปเรียกว่าแบตเตอรี่น้ำ (Storage Battery) ประกอบด้วยเซล 6 เซลล์ต่อกันแบบอนุกรม ซึ่งแต่ละเซลจะมีแรงดัน 2 โวลท์ จึงจ่ายแรงดันได้ 12 โวลท์ มีคุณสมบัติในการเปลี่ยนพลังงานเคมีแล้วจ่ายเป็นพลังงานไฟฟ้าชนิดกระแสตรง แบตเตอรี่ประเภทนี้ใช้งานจนไฟหมดหรือเลิกใชังานแล้ว สามารถนำไปประจุไฟเพิ่มเติมปรับสภาพทางเคมี ให้กลับสู่สภาพพร้อมใช้งานเหมือนเดิมได้ คือสามารถใช้หมุนเวียนได้จนกว่าแบตเตอรี่นั้นจะเสื่อมสภาพ แบตเตอรี่ชนิดนี้ส่วนมากทำจากตะกั่ว - กรด ใช้ในรถยนต์ และในการใช้พลังงานไฟฟ้าสำรองในระบบต่างๆ
.
.
.
แบตเตอรี่สะสมไฟฟ้าแบบตะกั่ว (Lead Storage Battery)
.
.........................แบตเตอรี่คือเซลล์ไฟฟ้าหลาย ๆ เซลล์ต่อกันเป็นอนุกรม แบตเตอรี่สะสมไฟฟ้าแบบตะกั่วนี้เป็นแบตเตอรีที่ใช้ในรถยนต์ โดยประกอบด้วยเซลล์ไฟฟ้า 6 เซลล์ แต่ละเซลล์จะมีศักย์ไฟฟ้า 2 โวลต์ ดังนั้นแบตเตอรี่ในรถยนต์มีศักย์ไฟฟ้า 12 โวลต์
.
.
.
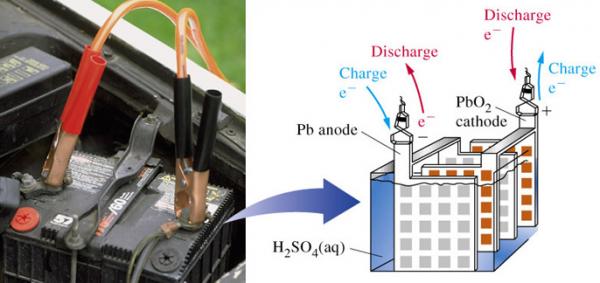
.
( ที่มารูป ::: http://lab.excise.go.th/image/bat2.jpg )
.
.
แบตเตอรี่ สะสมไฟฟ้าแบบตะกั่วจะประกอบด้วยอิเล็กโทรดคือแผ่นตะกั่ว มีกรดซัลฟิวริกเจือจางเป็นอิเล็กโทรไลต์ เมื่อมีการอัดไฟครั้งแรกแผ่นตะกั่วที่ต่อกับขั้วบวกของแบตเตอรี (ขั้วแอโนด) จะถูกออกซิไดซ์เป็นเลด (II) ไอออน ดังสมการ

เมื่อรวมกับออกซิเจนที่เกิดขึ้นจะกลายเป็นเลด (IV) ออกไซด์
.
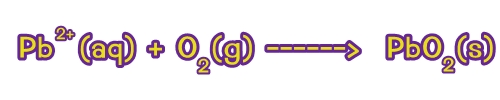
ดังนั้นที่ขั้วแอโนด (ขั้วบวก) แผ่นตะกั่วจะถูกเปลี่ยนเป็นเลด (IV) ออกไซด์ขั้วไฟฟ้าจึงแตกต่างกัน
(ขั้วแอโนด-ขั้วบวก: PbO2 และขั้วแคโทด-ขั้วลบ: Pb) ทำให้สามารถเกิดกระแสไฟฟ้าได้หรือจ่ายไฟได้นั่นเองการจ่ายไฟเกิดขึ้น ดังสมการ
.

.
.
อิเล็กตรอนจะเคลื่อนที่จากขั้วแอโนดหรือขั้วลบผ่านวงจรภายนอกไปยัง ขั้วแคโทดหรือขั้วบวก จากสมการจะสังเกตได้ว่ามีผลิตภัณฑ์คือ PbSO4(s) เกิดขึ้นเหมือนกัน ดังนั้นเมื่อใช้แบตเตอรี่ไประยะหนึ่งความต่างศักย์จะลดลง และจะลดลงไปเรื่อย ๆ จนกระทั่งเป็นศูนย์ ทั้งนี้เนื่องจากขั้วไฟฟ้าทั้งคู่เหมือนกัน จึงไม่มีความแตกต่างของศักย์ไฟฟ้าระหว่างขั้วทั้งสอง
.
ปฏิกิริยาของเชลล์ข้างบนเป็นผันกลับได้ ดังนั้นถ้าต้องการให้เกิดการผันกลับจึงจำเป็นต้องมีการอัดไฟฟ้าใหม่ โดยการต่อขั้วบวกของเซลล์กับขั้วบวกของแบตเตอรี่และขั้วลบกับขั้วลบของ แบตเตอรี่ ปฏิกิริยาข้างบนก็จะเปลี่ยนทิศทางเป็นจากขวาไปซ้าย ในลักษณะนี้เลด(II) ซัลเฟตที่ขั้วลบก็จะเปลี่ยนเป็นตะกั่ว ส่วนอีกขั้วหนึ่ง เลด (II) ซัลเฟตจะเปลี่ยนเป็นเลด (IV) ออกไซด์ ดังสมการ
ปฏิกิริยาของเชลล์ข้างบนเป็นผันกลับได้ ดังนั้นถ้าต้องการให้เกิดการผันกลับจึงจำเป็นต้องมีการอัดไฟฟ้าใหม่ โดยการต่อขั้วบวกของเซลล์กับขั้วบวกของแบตเตอรี่และขั้วลบกับขั้วลบของ แบตเตอรี่ ปฏิกิริยาข้างบนก็จะเปลี่ยนทิศทางเป็นจากขวาไปซ้าย ในลักษณะนี้เลด(II) ซัลเฟตที่ขั้วลบก็จะเปลี่ยนเป็นตะกั่ว ส่วนอีกขั้วหนึ่ง เลด (II) ซัลเฟตจะเปลี่ยนเป็นเลด (IV) ออกไซด์ ดังสมการ
.
.
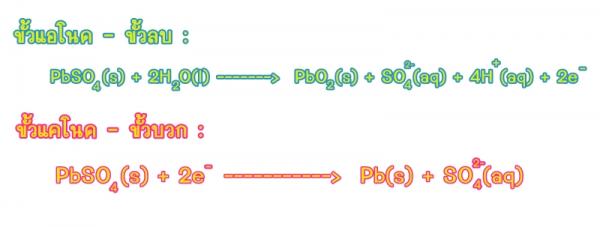
.
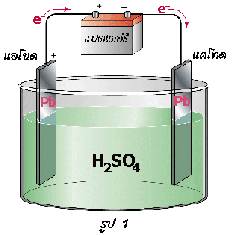
.
1) เมื่ออัดไฟครั้งแรก
.
.
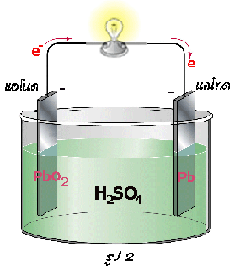
.
2) เมื่อจ่ายไฟ
.
.
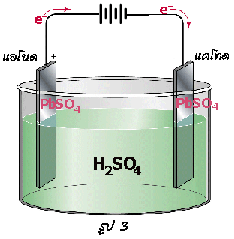
.
3) เมื่ออัดไฟครั้งต่อไป
.
.
* ขั้วบวก และ ลบ ของแบตเตอรี่
รูปที่ 1) และ 3) พิจารณาตามขั้วของแบตเตอรี่ภายนอก
รูปที่ 2) พิจารณาจากทิศทางการไหลของอิเล็กตรอน
รูปที่ 1) และ 3) พิจารณาตามขั้วของแบตเตอรี่ภายนอก
รูปที่ 2) พิจารณาจากทิศทางการไหลของอิเล็กตรอน
.
จากปฏิกิริยาในขณะที่มีการจ่ายไฟฟ้า ความเข้มข้นของกรดจะลดลงเรื่อย ๆ จากปกติที่มีความถ่วงจำเพาะ ประมาณ 1.25 ถึง 1.30 แล้วแต่อุณหภูมิในขณะนั้น ๆ ถ้าหากเมื่อใดมีความถ่วงจำเพาะต่ำกว่า 1.20 ที่อุณหภูมิของห้องก็ควรจะมีการอัดไฟฟ้าใหม่ได้
.
.
........ประโยชน์ของแบตเตอรี่รถยนต์มี 3 ประการ
.
1. จ่ายพลังงานให้สตาร์ทเตอร์และระบบจุดระเบิดของเครื่องยนต์ เพื่อให้เครื่องยนต์ทำงาน
2. จ่ายพลังงานส่วนเกินให้กับรถยนต์เมื่อการใช้ไฟฟ้าในรถยนต์เกินปริมาณที่ระบบ ชาร์จไฟในรถยนต์สามารถผลิตได้
3. รักษาระดับโวล์ทเทจของระบบไฟฟ้าในรถยนต์ให้คงที่ ช่วยป้องกันอุปกรณ์ไฟฟ้าไม่ให้เกิดความเสียหาย
1. จ่ายพลังงานให้สตาร์ทเตอร์และระบบจุดระเบิดของเครื่องยนต์ เพื่อให้เครื่องยนต์ทำงาน
2. จ่ายพลังงานส่วนเกินให้กับรถยนต์เมื่อการใช้ไฟฟ้าในรถยนต์เกินปริมาณที่ระบบ ชาร์จไฟในรถยนต์สามารถผลิตได้
3. รักษาระดับโวล์ทเทจของระบบไฟฟ้าในรถยนต์ให้คงที่ ช่วยป้องกันอุปกรณ์ไฟฟ้าไม่ให้เกิดความเสียหาย
.
.
.
แหล่งอ้างอิง
http://www.il.mahidol.ac.th/e-media/electrochemistry/web/secondary_cell.htm
http://www.expert2you.com/view_article.php?art_id=1883
http://lab.excise.go.th/group3/battery/batreac.htm
http://www.expert2you.com/view_article.php?art_id=1883
http://lab.excise.go.th/group3/battery/batreac.htm
.
.
.
.
.
.










