การแตกตัวของเบสอ่อน


![]() การแตกตัวของเบสอ่อน
การแตกตัวของเบสอ่อน
เบสอ่อนเมื่อละลายน้ำแล้วจะแตกตัวเป็นไอออนได้เพียงบางส่วนเช่นเดียวกับกรดอ่อน โดยปฏิกิริยาการแตกตัวของเบสอ่อนเป็นปฏิกิริยาที่ผันกลับได้ เช่น
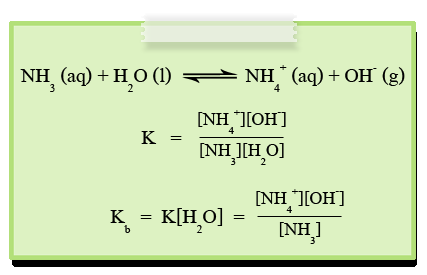
Kb คือ ค่าคงที่สมดุลของเบส ใช้ในการเปรียบเทียบความแรงของเบสได้เช่นเดียวกับค่า Ka
- โมโนโปรติกเบส (monoprotic base) สามารถรับ H+ ได้ 1 ตัว และมีค่า Kb เพียงค่าเดียวเท่านั้น เช่น NH3 เป็นต้น
- โพลิโปรติกเบส (polyprotic base) สามารถรับ H+ ได้มากกว่า 1 ตัว และมีค่า Kb ได้หลายค่า เช่น ไฮดราซีน (H2NNH2) เป็นต้น
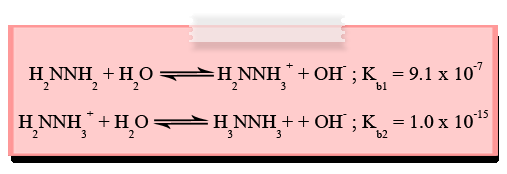
นอกจากนี้ค่า Kb ยังสามารถบอกปริมาณการแตกตัวของเบสอ่อนได้ในลักษณะเปอร์เซ็นต์ของการแตกตัว ดังนี้

![]() การคำนวณเกี่ยวกับค่าคงที่สมดุลของเบส
การคำนวณเกี่ยวกับค่าคงที่สมดุลของเบส
ตัวอย่างที่ 1 จงเขียนค่าคงที่สมดุลของเบสอ่อนต่อไปนี้ C6H5NH2 , N2H2
วิธีทำ
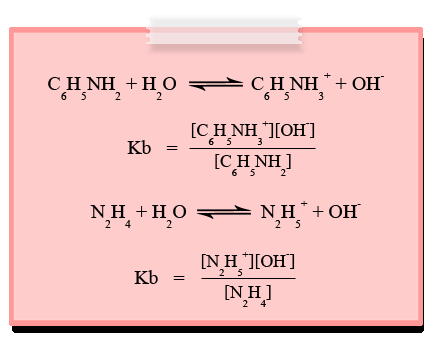
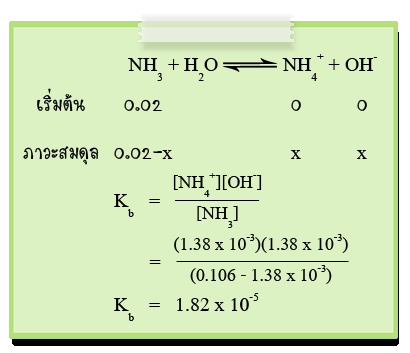
ตัวอย่างที่ 2 เมื่อแอมโมเนียละลายน้ำจะแตกตัวให้ NH4+ และ OH- ถ้าแอมโมเนียจำนวน 0.106 โมล ละลายในน้ำ 1 ลิตร ที่ภาวะสมดุลแตกตัวให้ NH4+ และ OH- เท่ากัน คือ 1.38 x 10-3 โมล จงหาค่าคงที่ของการแตกตัวของ NH3
วิธีทำ