การแตกตัวของกรดอ่อน


![]() การแตกตัวของกรดอ่อน
การแตกตัวของกรดอ่อน
สารละลายกรดอ่อน เช่น กรดแอซิติก (CH3COOH) เมื่อละลายน้ำแล้ว จะมีความสามารถในการนำไฟฟ้าได้น้อย เนื่องจากกรดแอซิติกนั้นแตกตัวเป็นไอออนได้เพียงบางส่วน เขียนแทนด้วยลูกศร ![]() เพื่อชี้ให้เห็นว่าปฏิกิริยที่เกิดขึ้นนี้เป็นทั้งปฏิกิริยาไปข้างหน้าและปฏิกิริยาย้อนกลับ โดยอยู่ในภาวะสมดุล เช่น
เพื่อชี้ให้เห็นว่าปฏิกิริยที่เกิดขึ้นนี้เป็นทั้งปฏิกิริยาไปข้างหน้าและปฏิกิริยาย้อนกลับ โดยอยู่ในภาวะสมดุล เช่น
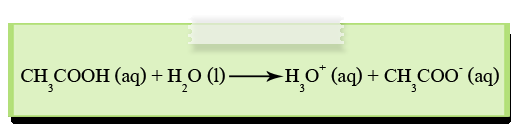
ปริมาณในการแตกตัวของกรดอ่อน นิยมบอกเป็นร้อยละ เช่น กรด HA แตกตัวได้ร้อยละ 10 ในน้ำ หมายความว่า กรด HA 1 โมล เมื่อละลายน้ำ จะแตกตัวให้ H+ เพียง 0.10 โมล

การแตกตัวของกรดอ่อนชนิดเดียวกัน จะเพิ่มขึ้นเมื่อสารละลายนั้นมีความเจือจางมากขึ้น เช่น กรดแอซิติก (CH3COOH) ความเข้มข้นต่างกันจะมีเปอร์เซ็นต์การแตกตัวต่างกัน ดังนี้

- การแตกตัวของกรดมอนอโปรติก (monoprotic acid dissociation)
กรดมอนอโปรติก คือ กรดที่แตกตัวให้ H+ ได้เพียง 1 ตัวเท่านั้น เช่น CH3COOH และ HCOOH
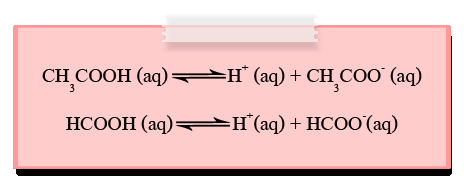
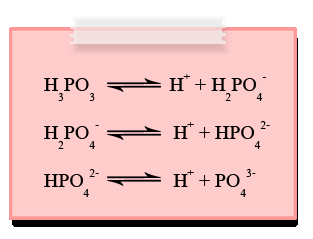
- การแตกตัวของกรดพอลิโปรติก (polyprotic acid dissociation )
กรดพอลิโปรติก หมายถึง กรดที่มีโปรตอนมากกว่า 1 ตัว และสามารถแตกตัวให้ H+ ได้มากกว่า 1 ตัว ถ้าแตกตัวแล้วได้ H+ 2 ตัว จะเรียกว่า กรดไดโปรติก เช่น H2CO3, H2S, H2C2O4 เป็นต้น
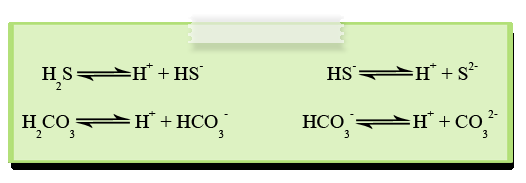
ส่วนกรดที่แตกตัวแล้วให้ H+ 3 ตัว เรียกว่า กรดไตรโปรติก เช่น H3PO4 , H3PO3