ทฤษฎีกรด-เบส(2)


![]() ทฤษฎีกรด – เบส ลิวอีส (Lewis)
ทฤษฎีกรด – เบส ลิวอีส (Lewis)
ในปี ค.ศ. 1923 (พ.ศ. 2466) ลิวอีส ได ได้เป็นผู้เสนอนิยามของกรดและเบส ดังนี้
กรด คือ สารที่รับอิเล็กตรอนคู่ แล้วเกิดพันธะโคเวเลนต์
เบส คือ สารที่ให้อิเล็กตรอนคู่ แล้วเกิดพันธะโคเวเลนต์
ปฏิกิริยาระหว่างกรด - เบส ตามทฤษฎีนี้ จะมีการใช้อิเล็กตรอนคู่ร่วมกัน โดยกรดจะเป็นผู้รับอิเล็กตรอน เรียกว่า Electrophile และเบสจะเป็นผู้ให้อิเล็กตรอน เรียกว่า Nucleophile ซึ่งตามทฤษฎีนี้สารที่เป็นเบสต้องมีอิเล็กตรอนคู่อิสระ เช่น
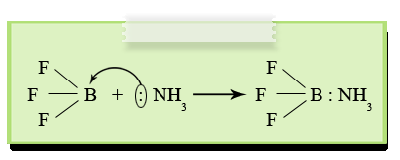
ดังกรณีนี้ NH3 เป็นเบสที่มีอิเล็กตรอนคู่อิสระ 1 คู่ จึงให้อิเล็กตรอนคู่กับกรดเพื่อทำให้เกิดพันธะโคเวเลนต์ ส่วน BF3 นั้นจะรับอิเล็กตรอนจาก NH3 ได้ผลิตภัณฑ์เป็น NH3BF3 ซึ่งมีสมบัติเป็นกรด
ทฤษฎีของลิวอิสนั้นมีข้อดี คือ สามารถจำแนกกรด - เบส ที่ไม่มีทั้ง H+ หรือ OH- อยู่ในสารนั้น และสารนั้นไม่จำเป็นต้องอยู่ในรูปของสารละลายเท่านั้น แต่ยังสามารถอยู่ในสถานะของแก๊สก็ใช้ทฤษฎีลิวอิสอธิบายความเป็นกรด - เบสได้
![]() สารที่เป็นได้ทั้งกรด – เบส (Amphoteric)
สารที่เป็นได้ทั้งกรด – เบส (Amphoteric)
สารบางตัวสามารถเป็นกรด เมื่อทำปฏิกิริยากับสารตัวหนึ่ง และเป็นเบส เมื่อทำปฏิกิริยากับอีกสารหนึ่ง หมายความว่าสารนั้นอาจเป็นได้ทั้งกรดและเบส โดยสารที่มีลักษณะนี้ เรียกว่า สารเอมโฟเทอริก (Amphoteric) เช่น H2O, HCO3- เป็นต้น
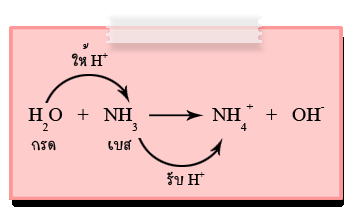
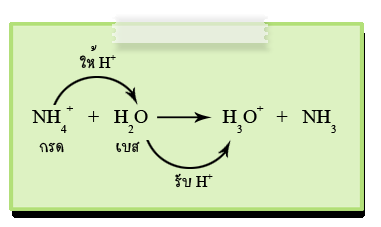
ในกรณีนี้ H2O จะเป็นกรดเมื่อทำปฏิกิริยากับ NH3 และจะเป็นเบสเมื่อทำปฏิกิริยากับ NH4+
ดังนั้นสามารถสรุปได้ว่า สารที่เป็นเอมโฟเทอริก เมื่อทำปฏิกิริยากับสารที่ให้โปรตอนได้ดีกว่า ตัวมันเองจะรับโปรตอน (เป็นเบส) แต่ถ้าไปทำปฏิกิริยากับสารที่ให้โปรตอนได้ไม่ดีหรือน้อยกว่า ตัวมันเองจะให้โปรตอนกับสารนั้น (เป็นกรด)